氮化硅是什么
氮化硅的首次制备工作是在1857年由亨利•埃蒂安•圣克莱尔•德维尔(Henri Etienne Sainte-Claire Deville)和弗里德里希•沃勒(Friedrich Wohler)完成的。在他们的方法中,将放入硅的坩埚放置在装有碳的坩埚内加热,以减少氧向装硅的坩埚的渗透。他们报告了他们称为氮化硅的产品,但没有确定其化学成分。保罗•舒泽伯格(Paul Schuetzenberger)首先报道了一种四氮化合物Si3N4,其在1879年通过在高炉中加热硅的填料而获得的。在1910年,路德维希•韦斯(Andyor Engelhardt)和西奥多•恩格尔哈特(Theodor Engelhardt)在纯氮气中加热硅来生产Si3N4。E. 弗里德里希(E. Friederich)和L.西蒂希(L. Sittig)在1925年通过在氮气下进行碳氮还原制备Si3N4,即通过在1250-1300℃下在氮气中加热二氧化硅和碳来制造Si3N4。
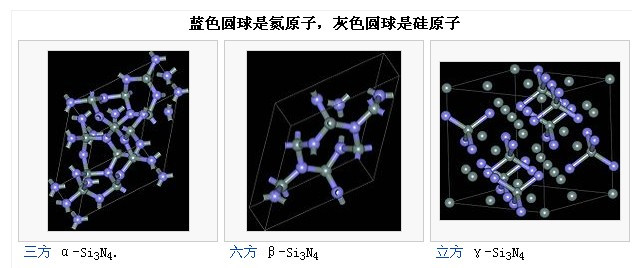
氮化硅属于无机非金属材料,化学式为Si3N4,是有三种晶型的共价键化合物,即α-Si3N4、β-Si3N4和γ-Si3N4。
物理性质
(一)组成与结构
氮化硅分子式为Si3N4,分子量为140.28,其中硅占60.06%(wt),氮占39.94%(wt)。由于两种元素的电负性相近,属于强共价键结合的化合物,所以氮化硅硬度高,熔点高,结构稳定,绝缘性能好。
Si3N4陶瓷属于多晶材料,常见的为α相和β相,均由[SiN4]硅氮四面体构成。结构上,β-Si3N4对称性较高,摩尔体积较小,是热力学稳定相。而α-Si3N4在动力学上比较容易生成,在高温下,α-Si3N4会发生重建式相变,转变为β-Si3N4,这种相变是不可逆的,因此高α-Si3N4粉有利于氮化硅陶瓷烧结。
(二)外观
不同晶相和工艺制备的氮化硅粉外观是不同的。α-Si3N4呈现白色或灰白色的疏松羊毛状或针状,氨解法制备的氮化硅粉呈白色或淡黄色的等轴状。β-Si3N4则颜色较深,呈致密的颗粒状多面体或短棱柱。高纯度的氮化硅单晶或晶须是透明或半透明的。氮化硅陶瓷也因工艺、用途和加入添加剂的不同而显示不同的颜色,从灰白、蓝灰、灰黑到近乎黑色。氮化硅陶瓷经抛光后有金属光泽。
(三)密度
Si3N4的理论密度为3.19±0.1g/cm3,实际测得的α-Si3N4密度为3.184g/cm3,β-Si3N4密度为3.187g/cm3。Si3N4陶瓷制品的密度与制备工艺及烧结助剂类别和添加量有关,因而有较大的变化范围。在相同的条件下,一般而言,热等静压烧结>气压烧结>热压烧结>常压烧结的密度。
(四)绝缘性
Si3N4陶瓷在常温和高温下都是电绝缘性的,其性能指标的优劣主要取决于合成方式与纯度。材料内的游离硅、碱金属、碱土金属、铁、铝、铜、钛、镍等金属杂质均可以劣化氮化硅陶瓷的电性能。Si3N4陶瓷在室温下、干燥介质中的电阻率一般为1015~1016Ω•cm,介电常数在4.8~9.5之间,介电损耗(1MHz)为0.001~0.1。
(五)热学性质
Si3N4属于高温难熔化合物,无熔点,常压下的分解温度为1900℃左右。只有在高于分解蒸气压444.8Pa的条件下,氮化硅才会熔融,这就是气压烧结氮化硅的基本原理。
25℃时氮化硅的比热为711.76/(kg•K),随温度升高而增大。Si3N4的热膨胀系数小,在(2.8~3.2)×10-6/K之间,随着Si3N4陶瓷密度和温度的增大而增大。
化学性质
机械性质
C-Si3N4结构
1999年德国和美国科学家共同报道了氮化硅的第三种晶型C–Si3N4(即γ-Si3N4)。它是在高温高压下合成的,具有立方尖晶石结构的氮化硅。